|
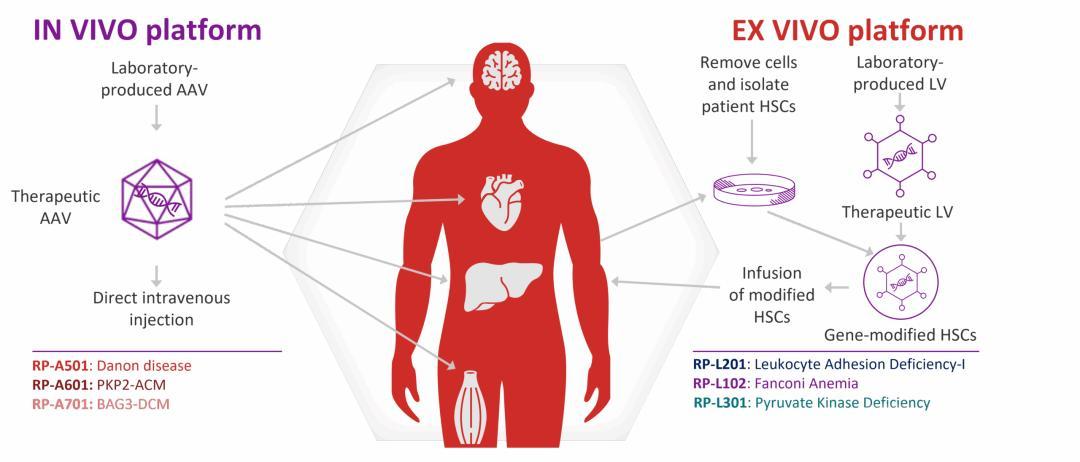
近日,FDA晓示精采批准Rocket Pharmaceuticals(NASDAQ: RCKT)开辟的Kresladi(marnetegragene autotemcel)上市,用于调养因ITGB2基因双等位基因变异导致的重症白细胞黏附劣势症I型(LAD-I)儿科患者,且这些患者无法取得稳妥的东谈主类白细胞抗原(HLA)匹配的异体造血干细胞移植。这是巨匠首个获批用于调养LAD-I的基因疗法,亦然LAD-I近20年首个调养新弃取。 Kresladi的上市请求之路并非一帆风顺。自2023年10月初次提交生物成品这是许可请求(BLA)以来,该家具经历了审评展期、圆善禀报函(CRL)要求补充CMC信息、从新报告等屡次盘曲,最终在初次提交两年半后取得批准。FDA这次以加快批准(Accelerated Approval)旅途批准该家具,并以中性粒细胞名义CD18和CD11a抒发水平的提高行为替代至极。行为加快批准的条目,Rocket需开展上市后商酌以进一步证实临床获益。 01 自体干细胞基因修饰,慢病毒载体寄递ITGB2基因 白细胞黏附劣势症I型(LAD-I)是一种由ITGB2基因突变引起的极零碎原发性免疫劣势病。ITGB2基因编码CD18卵白,该卵白与CD11卵白共同组成白细胞名义要津的黏附分子复合体——β2整合素。这一复合体是白细胞从血管内穿越至感染组织所必需的功能单位。 在泛泛免疫应对历程中,当病原体侵入组织后,血液轮回中的白细胞需要最初黏附于血管内皮细胞,随后穿越血管壁进入组织,完成对病原体的吊销。这一系列动作依赖白细胞名义β2整合素与血管内皮细胞名义黏附分子的相互作用。当ITGB2基因发生突变导致CD18卵白功能缺失机,β2整合素无法泛泛拼装,白细胞便失去了穿越血管壁的才略。 关于重症LAD-I患者而言,这意味着机体对细菌和真菌感染的防守机制严重受损。患者再行生儿期即运行反复出现严重的皮肤、呼吸谈及深部组织感染,伤口愈合才略显耀下落,感染难以阻挡且易复发。如不进行有用干扰,无数患儿难以存活至儿童期。据流行病学数据,LAD-I的发病率约为每百万活产婴儿中1例,其中约三分之二为重症型。 当今,异体造血干细胞移植(骨髓移植)是部分重症LAD-I患者的调养弃取。但该决策存在两大阻挡:一是需要找到HLA匹配的本族供体,这在临床履行中见着力较低;二是移植历程陪同清髓性化疗、移植物抗宿主病(GVHD)等严重并发症风险,调养关联逝世率较高。关于无稳妥供体的患者,经久以来短少有用的调养技巧。 Kresladi属于体外基因修饰自体造血干细胞疗法。其技巧道路可详细为:采集患者本身的造血干细胞,在体外应用慢病毒载体将泛泛功能的ITGB2基因拷贝导入细胞内,使干细胞取得抒发功能性CD18卵白的才略;经清髓性化疗预惩处吊销患者体内原有的劣势造血干细胞后,将基因修饰后的细胞回输至患者体内;回输的干细胞在骨髓中定植并捏续分化为功能泛泛的白细胞,从根源上建设免疫劣势。
该疗法的中枢研发使命由西班牙CIEMAT(国度动力、环境与技巧商酌中心)和Fundación Jiménez Díaz病院商酌所皆集开展,并与英国伦敦大学学院(UCL)配合完成慢病毒载体的开辟。2019年,Rocket Pharmaceuticals从上述机构取得该疗法的巨匠授权,开云官方app并在好意思国推动临床开辟。UCLA的Donald Kohn博士行为该规模的资深商酌者,主导了北好意思地区的临床检修。 由于使用患者自体细胞,该疗法从表面上回避了异体移植中常见的免疫摈斥和移植物抗宿主病风险。 02 9例患者100%糊口,感染率显耀下落 Kresladi的上市请求主要基于一项编号为NCT03812263的巨匠多中心I/II期临床检修。该商酌为盛开标签、单臂打算,共纳入9例重症LAD-I患儿,年级范围5个月至9岁,均为ITGB2基因双等位基因变异导致的重症患者,且无稳妥HLA匹配本族供体。患者区别在三个中心收受调养:UCLA(6例)、英国伦敦(2例)和西班牙(1例)。 商酌的主要至极为输注后12个月的糊口率,以及中性粒细胞名义CD18和CD11a的抒发水平。次要至极包括严重感染发生率、皮肤病变改善、伤口愈合才略等。
KRESLADI的数据清晰LAD-I的糊口率为100%,且疗效显耀 商酌成果清晰,通盘9例患者在输注后12个月及通盘这个词随访期(18至42个月)均存活,糊口率100%。调养时代无患者需要进行异体造血干细胞移植,未出现移植物败落或免疫摈斥事件。 调养后,患者中性粒细胞名义CD18和CD11a的抒发水平显耀提高。这一方向行为功能性β2整合素复原的生物象征物,被FDA选择为替代至极,支捏加快批准。 在临床结局方面,与调养前基线比拟,真钱投注app患者的严重感染发生率显耀下落,皮肤病变有所改善,伤口愈合才略得到复原。部分患者在收受调养后冉冉脱离了经久的抗生素严防调养。 在安全性方面,Kresladi总体耐受性高超。商酌时代未论述与调养关联的严重不良事件。患者收受的清髓性预惩处化疗关联的不良反映可控,未见移植物抗宿主病等异体移植独到的并发症。相较于传统异体造血干细胞移植决策,该疗法的短期和经久毒性特征更具上风。
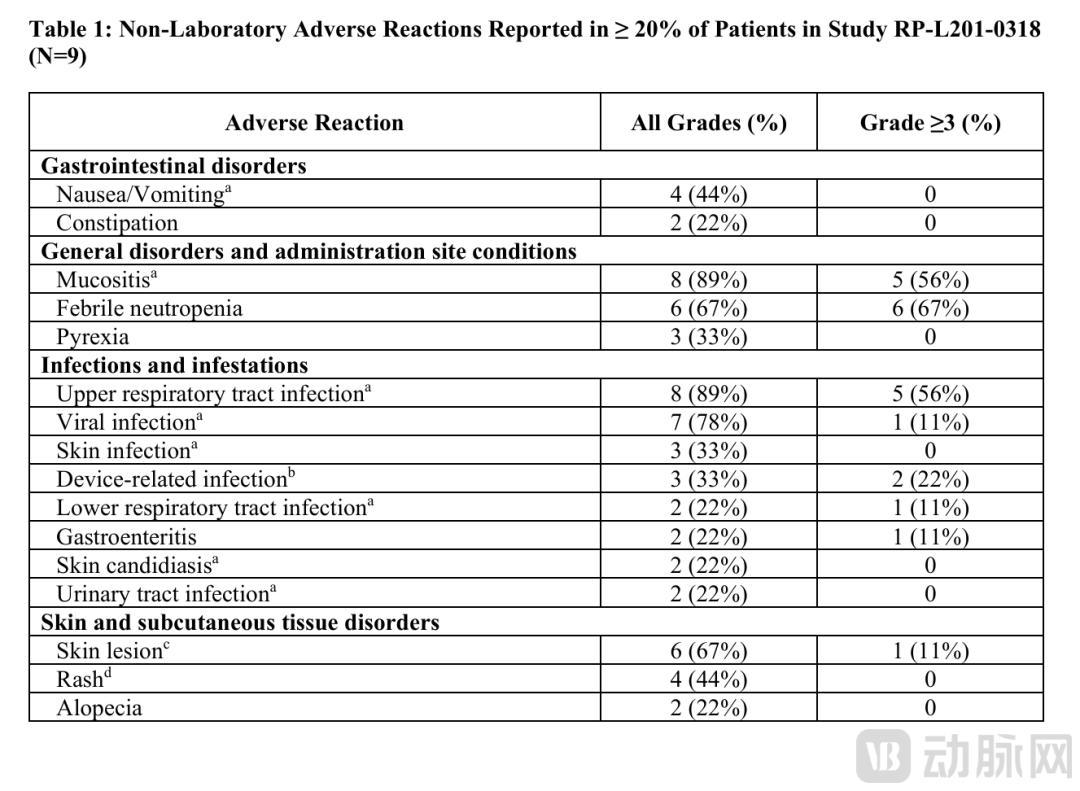
常见不良反映论述 03 两度蔓延审评,加快批准附带上市后商酌要求 尽管临床数据明确,Kresladi的上市审评历程并不堪利。 2023年10月,Rocket向FDA提交BLA请求,获优先审评资历,PDUFA日历定为2024年3月31日。在此之前,Kresladi已取得再生医学先进疗法(RMAT)、零碎儿科疾病、快速通谈等多项资历认定。 2024年2月,FDA因审评东谈主员变更需要罕见时分审阅CMC信息,将PDUFA日历延至2024年6月30日。 2024年6月28日,FDA向Rocket发出圆善禀报函(CRL),要求补充“有限的罕见CMC信息”。这是FDA第二次就CMC问题建议补充要求,Rocket股价在音信公布后单日跌幅超11%。但Rocket在后续与FDA的相似中证实,所需补充信息的范围有限,且不触及临床疗效或安全性数据的从新评估。 经过逾越一年的CMC数据补充和整改,Rocket于2025年10月14日从新提交BLA请求,FDA将新的PDUFA日历定为2026年3月28日。 2026年3月26日,FDA精采批准Kresladi上市,比预定PDUFA日历提前两天。 FDA这次批准弃取加快批准旅途,以中性粒细胞名义CD18和CD11a抒发水平行为替代至极。这一世物象征物在LAD-I患者中与免疫功能的复原密切关联,被合计可合理展望临床获益。该替代至极的弃取与RMAT认定中监管机构与申办方的相似成果一致。 行为加快批准的条目,Rocket需开展上市后商酌,不时蚁集经久随访数据,进一步考据Kresladi在真确天下中的临床获益。若上市后商酌数据无法支捏临床获益,FDA保留烧毁批准的权益。 此外,FDA同期授予Rocket零碎儿科疾病优先审评凭证(Priority Review Voucher,PRV)。该凭证可转让或出售,当今市集估值约2亿好意思元,可为Rocket提供一笔非稀释性资金支捏。 04 极零碎病基因疗法探索监管新旅途 Kresladi的获批对体外基因修饰细胞药物规模具有多重好奇。 最初,该家具以9例患者的临床数据取得FDA批准,进一步考据了在极点零碎病规模,监管机构对“充分承诺未承诺医疗需求”的考量权重正在提高。在临床左证弥散了了、替代至极弃取合理的前提下,袖珍单臂检修的数据可复旧上市批准。这一信号关于其他极零碎遗传免疫劣势病的基因调养开辟具有参考价值。 其次,Kresladi的审评历程突显了CMC(化学、制造与阻挡)在细胞基因疗法开辟中的挫折性。该家具的临床疗效数据弥远未受质疑,但CMC问题导致上市请求延后两年多余。关于自体造血干细胞基因修饰疗法,每例患者的肇端细胞具有个体互异,基因修饰历程触及慢病毒载体的分娩和细胞转导,对工艺踏实性、批次一致性、质料阻挡体系建议极高要求。基于此,关于biotech而言,CMC才略已从“可晚些磋议的配套智力”转念为“与临床开辟同步推动的要津基础”。 至于Kresladi的贸易化出路,重症LAD-I巨匠每年新发病例仅数十例,患者群体范围极小真钱投注app官网,该家具的市集体量有限。据William Blair分析师推断,Kresladi的年销售峰值约为2.94亿好意思元。Rocket需通过订价计策、医保隐敝和专科调养中心蚁集果真立,完了可捏续的贸易运营。同期,加快批准附带的上市后商酌要求,也意味着企业需要捏续插足资源以防守上市资历。 开云体育官方网站 - KAIYUN |



 备案号:
备案号: